MEZCLAS:
En las mezclas se pueden separar por medio de procedimientos físicos, sus composiciones son variadas y sus propiedades son variadas con relación a sus componentes.
Cualquier mezcla puede tener una composición variada, como los componentes de una mezcla están meramente colocados unos encima de otros así pueden retener sus propias propiedades químicas, los componentes de una mezcla se pueden detectar por medio de un microscopio o incluso a simple vista hay dos formas para poder clasificar una mezcla la primera es la mezcla heterogénea y la segunda es la mezcla homogénea.
MEZCLA HETEROGENEA:
Son aquellas que sus componentes están bien entremezclados y la composición esta misma en cada parte sin importa que la muestra se muy pequeña
Ejemplo:
MEZCLA HOMOGÉNEA:
Son aquellas que los componentes no se pueden distinguir regiones o partículas separadas aun usando un microscopio no se puede distinguir entre una sustancia homogénea, una mezcla homogénea también se puede llamar solución.
Ejemplo:
TÉCNICAS DE SEPARACIÓN:
Para analizar la composición de cualquier muestra, de lo que es una mezcla, primero separamos sus componentes por medio físico y luego identificamos cada sustancia individual, las separaciones físicas más comunes son: decantación, filtración, cromatografía y destilación.
Ejemplos:
Extracción: Se utiliza para separar mezclas sólidas. Se hace pasar repetidamente por la mezcla un solvente que ayude a la extracción de alguno de los dos sólidos. La extracción se hará cuando el solvente se agrega en frío para ello se utiliza un extractor soxhlet. Si el solvente se agrega en caliente, el método se llamará decocción.
Lixiviación: Se utiliza para separar mezclas solidas. Se coloca la mezcla dentro de un tubo por el cual se hace pasar repetidamente un solvente selectivo, para separar el sólido soluble y dejar dentro del tubo el sólido insoluble.
Tamizado: se utiliza para separar mezclas sólidas. se hace parar la mezcla a través de mallas de alambre de diferente tamaño.
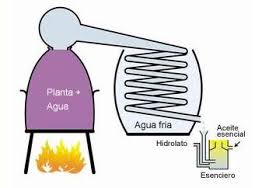
Destilación: se utiliza para separar mezclas liquidas. Se aprovecha el hecho de que cada líquido tiene un punto de ebullición determinado. La mezcla es colocada en un balón y se calienta hasta que se evapora uno de los los líquidos, luego pasa por un refrigerante y debido al descenso de temperatura brusco, el vapor se condensa separando así una mezcla.
Decantación: Se utiliza para separar mezclas liquidas ( en este caso heterogéneas). se coloca la mezcla en un embudo de separación que tiene en su parte inferior una llave de salida. se deja reposar aquella mezcla para que precipite el liquido más denso. luego se abre la llave y se deja salir el líquido de mayor densidad quedando así dentro del embudo el líquido menos solido.

Filtración: Se utiliza para separar mezclas heterogéneas de un sólido y un líquido. Se deja reposar la mezcla y luego se pasa esta misma a través de un filtro.
Evaporación: se utiliza para separar mezclas homogéneas de un sólido y un líquido. Se calienta la mezcla hasta que el líquido se evapore. separándose del sólido con el que se encontraba disuelto.

Cristalización: se utiliza para separar mezclas homogéneas de un sólido y de un líquido. Se disminuye la temperatura de la mezcla para que se cristalice el sólido. Luego se puede hacer la separación por filtración o decantación.

Centrifugación: Se utiliza para separar mezclas heterogéneas de un sólido y un líquido. Se coloca la mezcla en una centrífuga. Este precipita porque la fuerza de gravedad , lo cual facilita que la separación se haga mas rápida.

Cromatografía: Se utiliza para mezclas homogéneas entre sólidos, líquidos, gases y sólidos-Líquidos. el ejemplo mas simple es la cromatografía con papel. En un papel se coloca una pequeña muestra de la mezcla que se desea separar y se sumerge un extremo de éste en un líquido que hace las veces del solvente. el liquido "viaja" a través del papel y de acuerdo con las sustancias que allí se encuentren, se van separando, según sus pesos moleculares, quedando en la parte inferior del papel las más pesadas y en la parte superior las más livianas.
MOLARIDAD:
Es la concentración molar de un soluto en una solución, que común mente se denomina moralidad de soluto, es la cantidad de moléculas o formulas unitarias del soluto dividida por el volumen de la solución.
Formulas:
Las unidades de molaridad son moles por litro (mol∙L‾¹) y a menudo se indican como M:
1M = 1 mol∙L‾¹
El símbolo de M se lee con frecuencia "molarʺ. Note que 1mol∙L‾¹ es el mismo que 1mmol∙L‾¹. Los químicos que trabajan con baja concentraciones de soluto también informan concentraciones molares como millones por litro (1mmol∙L‾¹) y micro moles por litro (μ1mol∙L‾¹).
En el siguiente vídeo podemos observar que nos explican con cosas que hacemos diariamente en nuestros hogares las dos clase de mezclas tanto la mezcla homogénea como la mezcla heterogénea.









No hay comentarios:
Publicar un comentario